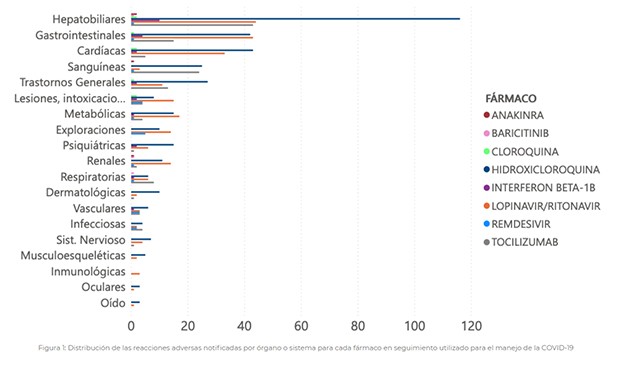
Reacciones adversas más habituales. Fuente: Aemps.
La
Agencia Española de Medicamentos y Productos Sanitarios (Aemps) ha registrado en la
base de datos Fedra un total de 305 sospechas de reacciones adversas producidas por los medicamentos en fase de prueba y seguimiento para el Covid-19.
-Sigue en directo las últimas noticias sobre la pandemia de coronavirus-
El fármaco que más sospechas de reacciones adversas ha generado es la
hidroxicloroquina. De los casos notificados, hidroxicloroquina aparece registrado como medicamento sospechoso en 234 casos, es decir, en e
l 76,7 por ciento de las ocasiones.
Le sigue
lopinavir/ritonavir, con 129 casos, y
tocilizumab con 74. Cifras inferiores presentan el
interferón beta 1B, con 12,
remdesivir con 11,
cloroquina con 5,
anakinra con 3 y
baricitinib con 1 caso.
"No se han recibido notificaciones con
interferón alfa 2B,
ruxolitinib,
sarilumab ni
siltuximab. Cabe esperar que los fármacos que más se administran sean los más notificados por lo que un mayor número de casos notificados no es indicativo de mayor riesgo", apunta la agencia en un comunicado.
Reacciones adversas más frecuentes
Las reacciones adversas más frecuentes detectadas en estos 305 casos son
hepatobiliares, gastrointestinales y cardiacas. Les siguen las reacciones sanguíneas, los trastornos generales y las intoxicaciones. Las menos frecuentes son de carácter inmunológico, oculares o afectan al oído.
Procedencia de los datos
De los 305 casos, 274 (90 por ciento) han sido notificados directamente a los
Centros Autonómicos de Farmacovigilancia y el 10 por ciento restante a través de la
industria farmacéutica. La mayoría han sido comunicados por profesionales sanitarios (299 casos, 98 por ciento) y 36 casos (12 por cientoi) proceden de estudios.
Las informaciones publicadas en Redacción Médica contienen afirmaciones, datos y declaraciones procedentes de instituciones oficiales y profesionales sanitarios. No obstante, ante cualquier duda relacionada con su salud, consulte con su especialista sanitario correspondiente.